
都说肝癌是“癌王”,得了肝癌,就等于判了死刑!可有人却偏偏不信,这不,PK“癌王”,市二医院就有新发现!
近日,在南京医科大学第一附属医院肝胆中心主任王学浩院士的带领和指导下,以王学浩院士作为通讯作者、倪勇教授作为共同第一作者(排名第二)的论文《HIF-1α-induced expression of m6A reader YTHDF1 drives hypoxia-induced autophagy and malignancy of hepatocellular carcinoma by promoting ATG2A and ATG14 translation》,在Nature系列期刊Signal Transduction and Targeted Therapy杂志(IF: 18.187)刊出,为肝癌治疗提供了新思路。

据介绍,N6-甲基腺苷(m6A)及其reader蛋白YTHDF1几乎影响RNA代谢的每个阶段,在人类肿瘤发生中发挥关键作用。自噬激活是癌细胞在缺氧状态下存活的途径之一。然而,在人肝细胞癌(HCC)中尚未探索m6A修饰在缺氧诱导的自噬中的可能作用。
该研究发现YTHDF1在HCC组织中的显著过表达与预后不良有关。多因素Cox回归分析表明,YTHDF1表达是HCC患者的独立预后因素。研究团队通过多种体内外模型(YTHDF1高表达/敲低/敲除细胞系、皮下成瘤模型、原位成瘤模型、类器官模型、患者来源异种移植物(PDX)小鼠模型以及基因敲除鼠模型)发现YTHDF1的表达与缺氧诱导的自噬显著相关,而下调YTHDF1的表达可抑制HCC的自噬、生长和转移。荧光素酶报告基因分析和染色质免疫沉淀表明,缺氧条件下HIF-1α通过直接与YTHDF1启动子区结合来调控其转录。MeRIP-Seq、蛋白质组学和多聚核糖体分析技术结果表明,YTHDF1通过与m6A 修饰的ATG2A和ATG14 mRNA结合,促进了自噬相关基因ATG2A 和ATG14的翻译,从而促进了肝癌自噬和自噬相关恶性生物学行为。
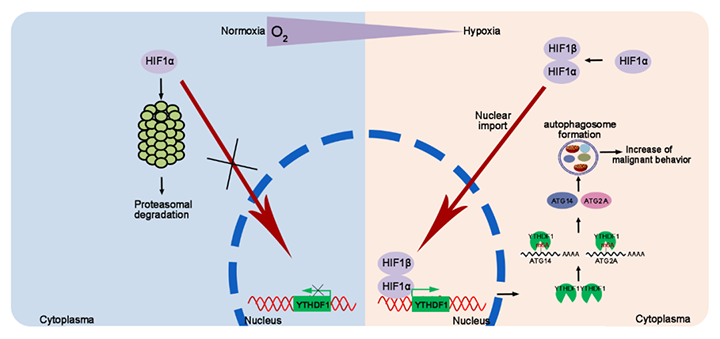
该研究创造了多个“首次”,包括首次揭示YTHDF1在HCC中的高表达与低氧诱导因子HIF1α对其转录调控有关;首次证实YTHDF1可以通过特异性识别甲基化修饰位点的方式,促进自噬相关蛋白ATG2A和ATG14的翻译,从而促进低氧诱导的自噬及自噬相关恶性生物学行为。这也证实了 YTHDF1是HCC患者的潜在预后生物标志物和治疗靶点。
该研究是深圳市第二人民医院通过深圳市“医疗卫生三名工程”引进南京医科大学第一附属医院王学浩院士肝胆中心团队后,科研上取得的喜人成果。
据介绍,南京医科大学第一附属医院(江苏省人民医院)肝胆中心是一个研究型的临床医学中心,是国家卫健委临床重点专科、中国医学科学院肝移植重点实验室,江苏省十大临床医学中心之一,是江苏国家级肝癌诊治中心,国内外享有盛誉。学科带头人为中国工程院院士王学浩教授,是我国著名的器官移植和肝胆外科专家,我国活体肝脏移植的开拓者,国际上肝癌现代介入治疗的开创人之一,我国肝癌介入治疗的先行者。 近年来,该中心先后获得国家重大研发计划1项,国家自然基金重点项目2项,国家自然基金项目共计33项,国家级及省部级科技项目资助经费累计约8000万元;在Science Translational Medicine、Hepatology、Journal of Hepatology、Science Signaling、Journal of Transplantation 、Journal of Immunology、Annals of Surgery等杂志上发表SCI论文约400余篇;先后获国家科技进步奖、省部级奖项10余项。
在“三名工程”的支持下,倪勇教授的团队有多名博士生,博士后在南京医科大学第一附属医院实验室进行共同合作,通过合作,科室也将不断强化科研能力,期待不久将来有更多的科研成果和文章发表。